NiFe-Hydrogenasen
Bis heute sind erst 4 Enzyme bekannt, die Nickel in ihrem aktiven Zentrum enthalten: Ureasen, Methyl-Cofaktor-M Reduktasen, Kohlenmonoxid-Dehydrogenasen und NiFe-Hydrogenasen. Im aktiven Zentrum der NiFe-Hydrogenasen finden sich neben Eisen-Ionen und säurelabilem anorganischem Schwefel auch Nickel-Ionen. Es handelt sich dabei meist um membrangebundene Hydrogenasen, die in den unterschiedlichsten aeroben, anaeroben und photosynthetisierenden Bakteriengruppen vorkommen.
Alle membrangebundenen und die meisten löslichen NiFe-Hydrogenasen bestehen mindestens aus einer großen und einer kleinen Untereinheit mit Molekulargewichten von jeweils 49 bis 86 bzw. von 15 bis 45 kDa. Die große Untereinheit dient dabei der Bindung des Nickels und der Wasserstoffaktivierung, während die kleine Untereinheit [Fe-S]-Cluster für den Elektronentransport enthält (Abbildung 2). Durch Röntgenstrukturanalyse konnte die Struktur von 2 NiFe-Hydrogenase aus der Gattung Desulfovibrio bestimmt werden. Danach ist das aktive Zentrum in der großen Untereinheit heterobinuklear und enthält neben Nickel noch ein Eisenatom. Abbildung 3 zeigt den Aufbau des aktiven Zentrums. Das Nickelatom ist über vier Cysteine quadrat-pyramidal koordiniert. Zwei davon dienen als Brückenliganden zwischen Nickel und Eisen, woraus ein Metall-Metall Abstand von 2,8 Angström resultiert. Das Eisen ist oktaedrisch gebunden. Die drei diatomaren Liganden konnten als 2 Cyanide und ein Kohlenmonoxidmolekül identifiziert werden.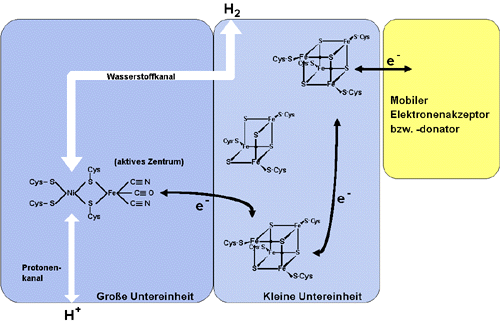
Abb. 2: Schematische Darstellung der NiFe-Hydrogenase aus Desulfovibrio gigas. Das [3Fe-4S]-Cluster ist wahrscheinlich nicht am Elektronentransfer beteiligt.
Der Vergleich mit Ni-Modell-Verbindungen sowie spektroskopische Daten (K-Kanten-Röntgenabsorptionsspektroskopie) lassen vermuten, daß das Nickel als Ni(I)-Ion vorliegt und während des Reaktionzyklus seinen Redoxzustand nicht ändert, wohingegen das Eisen redoxaktiv ist. Das Nickel wäre demnach nur zur Polarisierung des Wasserstoffs notwendig.
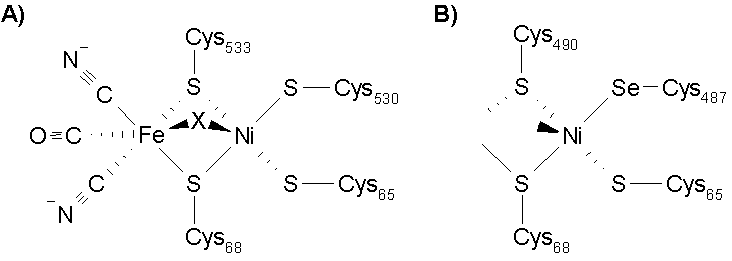
Abb. 3: Schematischer Aufbau des aktiven Zentrums A) der NiFe-Hydrogenase aus Desulfovibrio gigas und B) der NiFeSe-Hydrogenase aus Desulfomicrobium baculatum. X steht für das gebundene Hydridion. In B) sind nur die Liganden um das Ni-Atom eingezeichnet.



